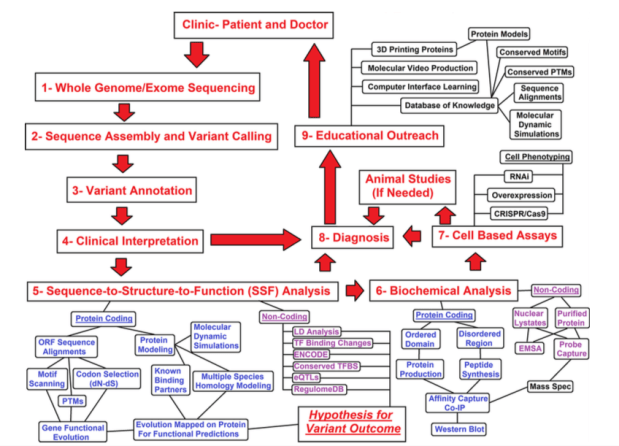
這篇是閱讀Adams, D. R., & Eng, C. M. (2018). Next-Generation Sequencing to Diagnose Suspected Genetic Disorders. N Engl J Med, 379(14), 1353-1362. doi:10.1056/NEJMra1711801的摘要。
Clinical Next-Generation Sequencing as Diagnostic tool
臨床次世代定序的使用越來越頻繁,不論是在神經基因體學,或是在小兒及新生兒急重症中都有所立足點,隨者世界各國不斷推行的大型計畫,未來定序技術在臨床上的服務會越來越重要。
美國:
Collins FS, Varmus H. A new initiative on precision medicine. N Engl J Med 2015;372:793-5.
中國:
Cyranoski D. China embraces preci- sion medicine on a massive scale. Nature 2016;529:9-10.
目前已有部分關於如何將基因資訊整合入臨床中的實務性建議和指引,畢竟在臨床導入的技術,需要嚴謹和品管的控制,以及可驗證性。
Bowdin S, Gilbert A, Bedoukian E, et al. Recommendations for the integration of genomics into clinical practice. Genet Med 2016;18:1075-84.
Beck TF, Mullikin JC. Systematic eval- uation of Sanger validation of next-gener- ation sequencing variants. Clin Chem 2016;62:647-54.
目前在一篇684個受測者的研究中,其分別使用外顯子測序和Sanger定序來比較受測者的五組基因,兩種技術的差異性可以接近99.97%。這研究顯示出目前測序技術的準確度越來越可靠。臨床應用測序技術的方式可以針對特定幾組基因或是整個基因組來定序,針對不同表型來設計相伴隨的測序基因組合。表型的範圍可以很小,也可以很大,小如familial hypercholesterolemia的四個基因組合,大的則如複雜疾病的表型,可以超過1000個基因以上的組合。
如何將這些應用於臨床決策這件事,到目前還是研究的熱點所在,相關的生物資訊工具還待開發與完善之中。最基礎的定序用是可以辨識基因序列中的序列變異(variants),並且取得其跟各種疾病相關的風險關聯,這部分在美國的ACMG指引中有提出如何系統性地來針對基因序列變異來產出報告。
Kalia SS, Adelman K, Bale SJ, et al. Recommendations for reporting of sec- ondary findings in clinical exome and genome sequencing, 2016 update (ACMG SF v2.0): a policy statement of the Ameri- can College of Medical Genetics and Ge- nomics. Genet Med 2017;19:249-55.
Variant Classification
如何將取得的基因變異序列(variants)資訊進行分類,便成為下一個重要的議題,通常一個檢體的基因變異位點可以有上千個以上,如何有效的過濾、排序來提供臨床闡述就很重要。這過程每個實驗室會稍有點不同,加上如何註釋資訊、如何闡述每個變異對於其他基因的影響,這類型通常都需要變一點跟疾病強烈的關聯,而這通常都沒有的。
變異位點的特性可以用演化保守性、族群頻率分析、或是以其所在的蛋白質功能來歸納。在大型定序資料庫Genome Aggregation Database(gnomeAD)中有提供常見變異(Common Variants)和罕見變異(Rare Variants)。目前美國醫學遺傳學會有提供一個指引用來將變異分類成:pathogenic, likely pathogenic, likely benign, benign, 和variant of unknown significance等幾種歸類。
Richards S, Aziz N, Bale S, et al. Stan- dards and guidelines for the interpreta- tion of sequence variants: a joint consen- sus recommendation of the American College of Medical Genetics and Genom- ics and the Association for Molecular Pa- thology. Genet Med 2015;17:405-24.
在另一個重要的資料庫ClinVar中,還會將這些基因變異位點跟臨床表型連結在一起。算是更一進步把變異點跟已知道許多臨床表徵會結再一起,雖然其中會有許多重疊之處。當實際將次序導入臨床實務時,會隨之產生許多新的gene-disease關聯出現,其中偽關聯不可避免地出現,一些新的工具可以幫助我們將外部資料庫的案例匯集一起來減少偽關聯,如Gene- Matcher (https://genematcher.org/), DECIPHER (https://decipher.sanger.ac.uk/), Phenome- Central (https://www.phenomecentral.org/) 。
MacArthur DG, Manolio TA, Dim- mock DP, et al. Guidelines for investigat- ing causality of sequence variants in hu-man disease. Nature 2014;508:469-76.
Diagnostic Rate and Stratedge
Implementation of Clinical Next Generation Sequencing
Reimbursement
Studies of Clinical Usefulness
Challenges and Opportunities
Health Person
Future directions