七月底利用時間請假去參加了台大生物技術研究中心舉辦的臨床次世代定序實務與應用課程,由郭靜穎、楊雅倩和蘇剛毅老師所舉辦的,整個課程蠻扎實的,台灣的確需要多一點這類課程,當初主要是對其hands-on的建庫課程感興趣,畢竟這類機會不多,通常都是廠商幫忙完成,所以想辦法實際來碰一下,順便看一下台大醫院這邊基因檢測的概況,課程表如下,分成兩塊:上課以及實作兩個部分,上課部分則是從基本次世代定序介紹到各主題如遺傳、癌症、微生物體、人類白血球抗原分型、次世代定序的法規、確校及認證以。實作部分則是做人類白血球抗原分型搭配和生物資訊分析,很開心能在持續精進,抱持者Rookie spirits,畢竟日新月異,還是一段時間得學習一番,當然不可能什麼都懂,但是至少多聽聽不同人切入次世代定序的看法!
全程可以看到郭靜穎老師辛苦的陪伴,郭靜穎老師在台大醫技系畢業後,至美國加州希望之城生物科學研究所攻取博士學位,然後在希望之城糖尿病與代謝研究中心做博士後研究員,博士後研究結束之後,其在希望之城醫學中心的臨床分子檢驗實驗室做基因變異分析師,然後2017年回來台灣大學醫學檢驗暨生物技術學系做老師,所以課程中也可以聽郭老師分享美國臨床分子檢驗室的架構,聽完覺得要建立一個一流的分子醫學檢驗實驗室真的不簡單,需要非常多不同專長的人員,另外令我很佩服的是楊雅倩老師,楊雅倩老師是台灣檢驗醫學界很資深的教授,但她也是趁者空擋基礎全程參與從做實驗到生物資訊分析,看著老師自己打開筆電跟者學習怎麼使用生物資訊軟體甚至程式碼的輸入,這精神真的值得學習,希望能持續保持如楊雅倩老師這種學習精神!

其中陳沛隆醫師的課程提到蠻多很珍貴的觀點,次世代定序在台灣已經談論快十年,尤其最近五年在台灣做定序的價錢已經很便宜了,往往會給人一種好像這個工具無堅不摧(當然不是,每個檢驗技術都有優點和缺點),陳沛隆醫師則願意分享其看到的機會:
- Reference genome: population-specific?
- Haplotyping/phasing
- Psudogene
- Structural variation (SV)
- Dynamic mutation
- Mobile element
- Somatic mutation
- Digenic/oligogenic mode
- Epigenetic change
- Non-coding region (such as TAD, UTR, etc.)
上面是完整寫下陳沛隆醫師簡報裡面的字串,可惜時間不足,所以陳醫師沒有辦法一項項細講,感覺裡面滿滿的珠璣!這邊趁機來查一下:
參考基因組在次世代定序中的影響
之前在科內晨會就準備過這個主題,所以可以理解陳醫師的意思!

參考基因組在第二代定序(所謂的次世代定序中)影響頗大,基本上可以暱稱次世代定序為高通量短片段定序,所以參照的拼圖對於把讀長序列(reads)排序回去就變得異常重要,而目前我們所謂的參考基因組主要是使用美國人類基因組計畫中所產生的參考序列其實從2003年的草稿到今天為止,存在很多問題(科學就是越探索,越發現事情比想像中複雜ORZ),美國人類基因組計畫中所使用的檢體其實並非一個人的檢體,而是一群人,然後把它分發給世界各地合作對象來定序,下面是當初的招收廣告:

這是當初刊登在報紙上徵求自願者時候的廣告,蠻有趣的,當初要的是20個人,不過後來我們發現其實實際基因體系列可能大多數是某一位自願者的檢體,且實際可能有約30個人左右

直到今年2021年六月我們才有一個比較接近完整的人類基因組定序取得,是由Telomere-to-telomere consortium團隊所發表的,他們利用了很多第三代定序的技術來混合完成這個任務的,這篇論文The complete sequence of a human genome目前是發表在bioRxiv上面,可以由這篇Nature新聞A complete human genome sequence is close: how scientists filled in the gaps了解這件事代表,另外,他們所使用的定序檢體也很特別,是使用hydatidiform mole,也就是將精子注射到一個沒有核的卵子中,這樣可以一次定序一股染色體,不用面對phasing的問題。
Pseudogenes對於短序列alignment的影響
這也是之前有概念,但沒有特別關注的議題,實際去調查真的發現蠻有趣的,所謂的假基因(Pseudogenes)是染色體上的基因片段,其跟對應的基因相似,但可能散失部分功能,目前認為他可能是細胞複製過程所產生的重複序列,在探討演化的學者這個現象很重要,可以利用Pseudogene的片段來探討種源的距離,這邊因此可以理解到這個Pseudogenes會如何影響到定序結果,一方面是來自Pseudogene的reads可能會被貼到其同源基因區域,或是者反之也會發生(OS:好複雜,難怪很多時候即時有定序資料還是看不出什麼所以然,很多因此會影響結果),在Nature Reviews Genetis 2020年12月後有一篇Overcoming challenges and dogmas to understand the functions of pseudogenes在談論如何研究pseudogene以及他在生物學的角色。
實務上來說,蠻多臨床上重要的基因就有很多這類同源基因,比如PMS2, CYP2D6, CHEK2, SMN1, PKD1,這邊就有一個這類對於二代定序和Sanger定序都是所謂盲點的基因列表:
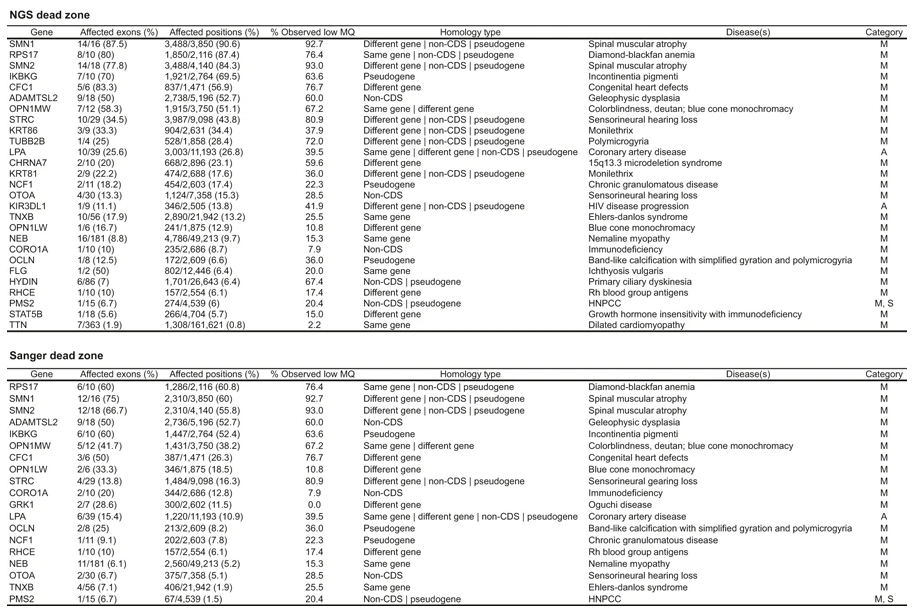
短片段定序無法偵測之基因變異
知道越多人類序列,才發現人類序列的變化遠比想像的多,從下面的圖可以知道像是Structural variation, Repeat expansion以及所謂Phasing的問題都是目前二代定序的工具無法解決的。

有的基因變異的範圍很方式其實是比想像中多的,從上面的Structural variation也可看到如reverse或是translocation這類的轉位,短片段的序列都還是能得到,但是alignment會去參考基因組時,就看不到這樣的資訊,以前覺得沒有太大影響,但後來發現這些都多多少少造成其基因表現的不同。
動態突變 Dynamic mutation:短片段重複相關的疾病disorder
動態突變造成的疾病也是之前我不太懂的,仔細一查,維基百科的定義是:
an unstable heritable element where the probability of expression of a mutant phenotype is a function of the number of copies of the mutation. That is, the replication product (progeny) of a dynamic mutation has a different likelihood of mutation than its predecessor
from Dynamic mutation, Wiki
不過目前比較常用Trinucleotide repeat disorder來形容,跟此相關的疾病也不少,最知名的就是亨廷頓舞蹈症,當然還有蠻多跟此相關的疾病:


這類疾病可能使用NGS在定序時,因為參考基因組的關係,可能不容易檢測到,在一般的alignment分析中應該也不容易排列好,看起來也不是很容易被探討的疾病種類。不過幾篇文獻看起來是特別的一群基因疾病
- Mirkin, S. Expandable DNA repeats and human disease. Nature 447, 932–940 (2007). https://doi.org/10.1038/nature05977
- Usdin K, House NC, Freudenreich CH. Repeat instability during DNA repair: Insights from model systems. Crit Rev Biochem Mol Biol. 2015;50(2):142-167. doi:10.3109/10409238.2014.999192
- McIvor EI, Polak U, Napierala M. New insights into repeat instability: role of RNA•DNA hybrids. RNA Biol. 2010;7(5):551-558. doi:10.4161/rna.7.5.12745
- Li, D., Pan, S., Zhang, H. et al. A comprehensive microsatellite landscape of human Y-DNA at kilobase resolution. BMC Genomics 22, 76 (2021). https://doi.org/10.1186/s12864-021-07389-5
- Ajjugal, Y., Kolimi, N. & Rathinavelan, T. Secondary structural choice of DNA and RNA associated with CGG/CCG trinucleotide repeat expansion rationalizes the RNA misprocessing in FXTAS. Sci Rep 11, 8163 (2021). https://doi.org/10.1038/s41598-021-87097-y
從下面的圖也可以看出來在不同基因甚至區段上面的這種重複序列,可能跟不同的疾病相關連,看到這邊真的驚嘆人類基因體的奧秘,另一個角度來看,人類的疾病也可以看成是基因多型性的一種表現吧!
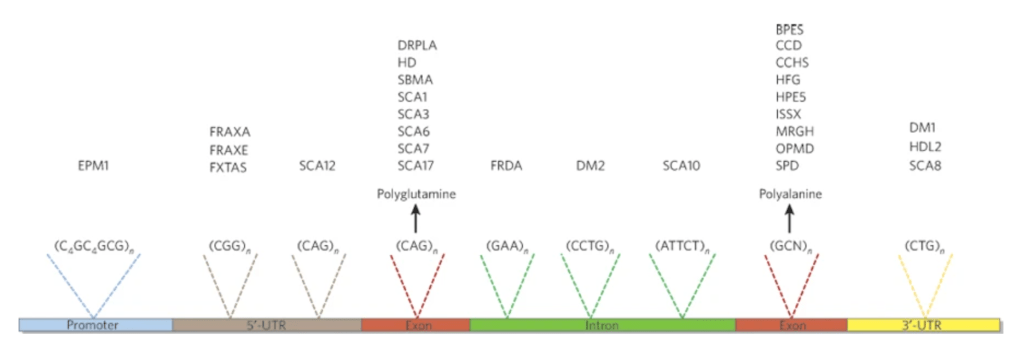
雙基因或多基因遺傳模式(Digenic/Oligogenic Mode)
顧名思義就是某一個性狀是由多個基因所造成的,所以當同時有兩個變異發生在兩個基因上時就會造成某個性狀產生,這時候可以稱為Digenic inheritance,這類在之前也是比較少見(當然也是武器不夠好),慢慢也開始有一些文章開始探討!
- A genome-wide case-only test for the detection of digenic inheritance in human exomes. PNAS. 2020, 117 (32) 19367-19375; DOI: 10.1073/pnas.1920650117
- The digenic causality in familial hypercholesterolemia: revising the genotype – phenotype correlations of the dsiease. Front Genet. 2021. https://doi.org/10.3389/fgene.2020.572045
- Genetic modifiers and oligogenic inheritance. 2021. Cold Spring Harbor Perspectives in Medicine
- Digenic inheritance and genetic modifiers. Clinical Genetics. 2018. https://doi.org/10.1111/cge.13150
陳沛隆醫師所列出的每一點都有蠻多可學習的地方,也可以一窺所謂遺傳基因體學的面貌!


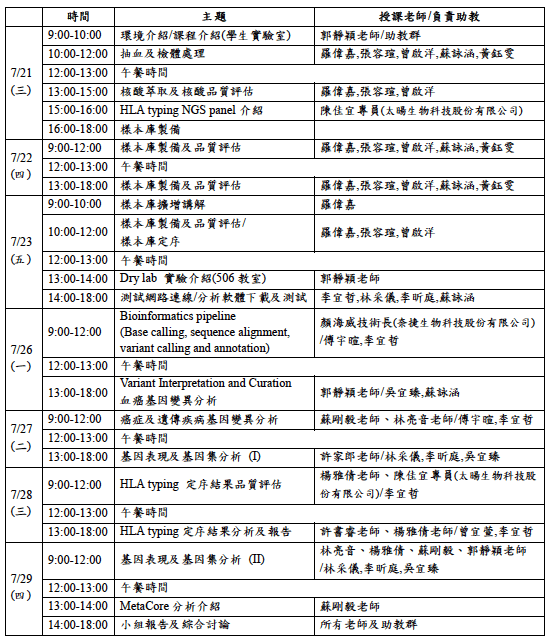
2023的郭靜穎老師依舊用心,課程整體依舊扎實阿~
讚讚