當超音波走進醫學美容:2025 白話超音波輔助醫美療程系列課程回顧
在一開始進入自費領域時,選擇以醫學美容為切入點,那時候觀察到的問題是標準化治療遇到客人個體化差異的問題,尤其很多儀器和工具幾乎都是廠商的教學為主,有時候講解的內容不太能說服我,比如最常見4.5mm打筋膜這件事情,實務上,每個人臉筋膜區都不同,甚至同一張臉筋膜結構都不同,以臉部為例,這是個全身軟組織變化度與組織細緻度最高的地方,而我希望能有更客觀的資訊去做評估,雖然基本上肉眼、觸診搭配一些表情變化的觀察與過去病史可以解決大部分的問題,但許多細微的狀況是需要更多資訊來做評估,甚至我慢慢發現醫美的重點之一其實是診斷與治療計劃的安排,這兩件事需要的就是越多資訊越好,於是我便在找尋適合的工具來參與,手持式超音波便成為我的首選,而手持式超音波開始有許多很好的選擇,甚至有台灣自製的超音波,結合在地廠商來解決醫學問題是我覺得很棒的模式,相對使用國外代理的工具,有在地廠商協作通常可以發揮更大的效應,於是如同之前….喜愛故意多走一步挑戰自己的個性,開始自己花錢買超音波來鑽研。
一開始很怕會造成現場的診察流程太慢,還好慢慢地……發現我本來就很慢,也傾向於討論得很精準。


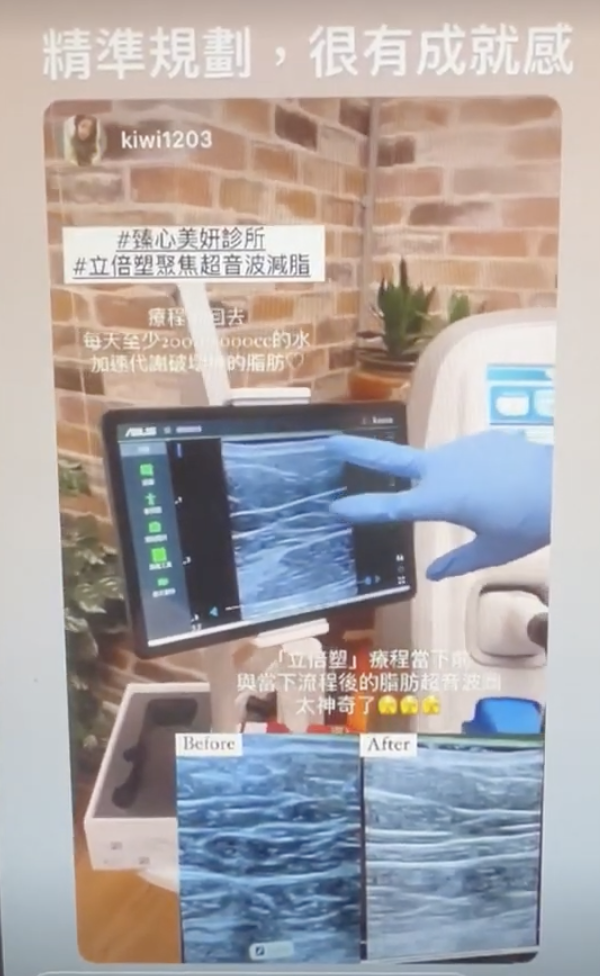

當時我調查一下在醫美領域實際用超音波於醫美的現況,其實使用率很低,大部分超音波在學術上主要用來解決併發症處理,這樣的使用機率就變得很局限,另一方面,許多醫美機構講究速度,且在連鎖醫美體系主流的時代,醫師相對來說無法改動太多臨床診察模式,於是剛好利用自己所待的診所的自由度,和診所老闆的支持,開始大量在看診時使用,隨者使用的量增加,也會增加很多有趣的臨床想法,這種回饋感是我很喜歡的,不斷從小細節中來進步,一方面可以提供更好的診斷,另一方面,也不斷發現新的現象,如今回頭看,醫美領域的變化,開始擺脫流水線的模式,進入精緻與客製化,這塊一定會慢慢變成顯學。
在2025年中的時候,診所老薛開始提及能不能讓我教其他醫師超音波的使用心得,我想說趁勢勇敢的跟廠商提議直接規劃成工作坊,逼迫自己更積極的使用與把心得總結成對其他醫師有用的資訊,於是在2025年末歸化城三堂系列課程的形式,帶領小班制的學員們一起探索手持式超音波在醫美領域的臨床應用。這篇文章是一份課後回顧,也是對這段教學歷程的紀錄與反思。今年預計也會在籌辦,就用這篇做一個總結,再往前進。
為什麼醫美需要超音波?
我自己的感覺是當我開始用超音波在進行醫美診察,有種把“醫療”專業帶進去我的實踐之中,因為我可以更客觀的給予評估,同時能看到這客人過去組織做的事情,且這些客觀資訊是客人或是患者也可以看到的,老實說,這讓看診變得很有成就感,也很系統性。
學術一點或是官方一點的說法,為何醫美需要超音波評估,主要是醫學美容療程——無論是電音波、肉毒桿菌素注射、填充物施打,還是埋線拉提——都涉及對於臉部結構的理解。傳統上,我們依賴解剖知識與觸診經驗來判斷注射深度與位置,但每個人的血管走向、脂肪墊厚度、肌肉型態都存在個體差異,這些差異正是併發症發生的主要風險來源,另一方面,廠商說的什麼深度用什麼治療,其實客人間的差異是巨大的。
超音波影像的價值在於,它讓我們「看見」皮膚底下正在發生的事,對於追求安全與精準的臨床醫師而言,這不是錦上添花,而是一項日益重要的基本功。
參考國外的超音波醫美課程
而去設計這樣的課程,知道最重要的是不要自己重新做輪子,所以發現目前國外超音波課程主要有Dr. Leonie Schelke和Dr. Peter Velthuis、Dr. Barbara Parda,他們有一套教學網站和實體課程,先從線上課程的方式去觀摩,他們的架構是比較偏向對解剖學結構的理解,當然一開始我也只能從這個角度來了解,不過慢慢地發現其實有更多的可能性,比如治療前的診斷工具或是規劃工具,這塊就增加很多能讓療程效果和安全更好的能力。
課程設計理念:從下往上,由淺入深



這次系列課程以「白話」為核心精神——希望將複雜的超音波解剖與操作技巧,用直觀、易懂的方式傳達,且希望能擺脫教科書的方式,直接講實用的地方,整合成臨床模塊,也花了蠻多時間,把實際使用時得到的心得實際使用出來。課程依照臉部區域分為三堂,從下半臉一路講到上半臉,每堂課都包含三個核心環節:解剖講解、臨床應用討論、以及 Hands-on 實作,在過程中,我自己也獲得很多,也產生一些新的想法。
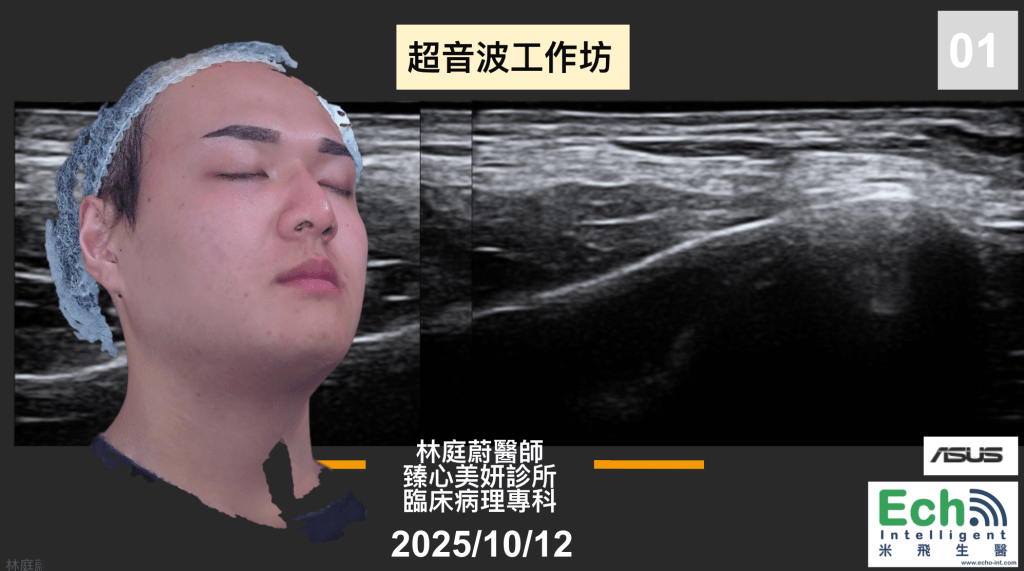
第一堂:下半臉(10/12)
下半臉是許多醫美療程的熱門區域,也是血管併發症的高風險區。這堂課聚焦在幾個關鍵結構:咬肌(masseter)的超音波下型態辨識與分型量測、闊頸肌(platysma)的走向,以及顏面動脈(facial artery)的路徑變異。
在臨床應用層面,我們討論了肉毒瘦臉時如何透過超音波確認咬肌厚度與邊界,以及拉提療程中如何利用影像避開重要血管。實作環節讓學員親手操作探頭,練習咬肌的分型量測——這是一個看似簡單、實則需要反覆練習才能掌握的技能。
第二堂:中臉(11/16)
中臉的解剖結構更為複雜,脂肪墊層次分明、動態肌肉交錯其間。這堂課我們深入探討了中臉脂肪墊(malar fat pad、buccal fat pad 等)的超音波辨識,以及動態肌肉在不同表情下的即時影像變化。
應用面則著重在僵化毛毛蟲(tyndall effect / filler migration)的超音波下表現與處置策略。填充物注射後的異常堆積,在超音波下有其特徵性的影像表現,這對於後續處理方案的制定非常有幫助。實作部分,學員練習了眼下結構的量測,以及填充手術前的評估與規劃。
第三堂:上半臉(12/21)
上半臉涵蓋額肌(frontalis)、顳部(temple)以及眉弓上方的 ROOF(retro-orbicularis oculi fat)等結構。這些區域在肉毒注射與填充治療中都有其獨特的挑戰:額肌的厚度與活動度直接影響肉毒劑量的選擇,而顳部的血管走向(特別是淺顳動脈及其分支)則是填充治療的安全關鍵。
臨床應用部分,我們討論了額頭眉弓治療設計與夫妻宮(temple)注射的超音波輔助策略。實作環節則聚焦在額肌分型——不同患者的額肌型態差異顯著,這直接影響治療方案的選擇。
回顧與展望
三堂課從下半臉到上半臉,我們建立了一套以超音波為核心的臉部解剖評估框架。但這只是起點。超音波在醫美領域的應用仍在快速發展中——從注射前的解剖評估、注射中的即時引導,到注射後的併發症偵測與處理,每一個環節都有超音波可以著力的空間。
身為臨床醫師,我相信「看得見」是「做得好」的前提,期待未來能繼續透過課程與臨床實踐,和更多同道一起推進超音波在醫美安全領域的應用,今年拜託剛從英國回來的林口長庚整形外科學長毛士軒醫師來指導,看能不能更來精進這個領域。
不過很開心,能跟隨自己的好奇,好好的把事情做好,當然也要很多工作上夥伴的支持
我幫你把所有本地路徑(反引號內的路徑字串)清除,保留其他所有內容。這是純文字格式的整理,不需要建立 docx。我直接把所有反引號路徑字串清除後輸出整理好的內容:
參考文獻
1. 超音波教科書 / Ultrasound Textbooks
- Nelson BP, Topol E, Bhagra A, et al. Atlas of Handheld Ultrasound. 1st ed. Springer International Publishing; 2018. ISBN: 9783030088712.
- Creditt A, Tozer J, Vitto M, Joyce M. Clinical Ultrasound: A Pocket Manual. 1st ed. Springer International; 2018. ISBN: 9782017961314.
- Hoskins PR, Martin K, Abigail T (eds). Diagnostic Ultrasound: Physics and Equipment. 3rd ed. CRC Press (Boca Raton); 2019. ISBN: 9780367190415.
- Woodward PJ, Griffith JF, Antonio GE. Imaging Anatomy: Ultrasound. 2nd ed. Elsevier; 2018. ISBN: 9780323548007.
2. 超音波臉部解剖 / Ultrasonographic Facial Anatomy
- Kim HJ, Youn KH, Kim JS, Kim YS, Hong SO, Na J. Ultrasonographic Anatomy of the Face and Neck for Minimally Invasive Procedures: An Anatomic Guideline for Ultrasonography. 1st ed. Springer (Singapore); 2021. ISBN: 9789811565595.
- Urdiales-Gálvez F, et al. Ultrasound in aesthetic dermatology (2021). J Cosmet Dermatol. 2021.
- Ingallina F, et al. (2022).
超音波系列綜述 (Diagnostics 期刊)
- Ultrasonography of the upper face. Diagnostics. 2024;14:1718.
- Ultrasonography of the middle face. Diagnostics. 2024;14:2544.
- Ultrasonography of the lower face. Diagnostics. 2025;15:921.
- Overall diagnostics review. Diagnostics. 2024;14:1718.
3. 下半臉:咬肌 / Lower Face — Masseter
- Lee HJ, et al. (2019).
- Masseter muscle and botulinum toxin. Toxins. 2017;9:14.
- Masseter-related review. Toxins. 2021;13:28.
- Masseter-related study. JOCD. 2024;24:e70301.
- Masseter-related review. Curr Pain Headache Rep. 2012;s13671-012-0013-y.
- Ultrasound study on masseter muscle. Sci Rep. 2020;10:s41598-020-71378-z.
4. 下半臉:頸部、闊頸肌、頦下 / Lower Face — Cervical & Submental Region
- Anatomy of the cervicomental region: insights from ultrasonography.
- Kochuba L, et al. (2020).
- Wollina U, et al. (2020).
- Age-related changes in lower facial fat compartments and blood vessels.
5. 中臉:脂肪墊、填充物、注射安全 / Mid Face — Fat Pads, Fillers & Injection Safety
- Rohrich RJ, et al. (2008). Fat compartment anatomy.
- Micheels P, et al. (2017).
- Polselli R, et al. (2017).
- Levesque AY, et al. (2015).
- Mertens DF, et al. (2016).
- Shin KJ, et al. (2018).
- Wen GD, et al. (2019).
- Anatomic study of fillers: mimetic injections for maximum safety.
- Anatomic study of fillers (duplicate copy).
- Importance of choke vessels in injectable fillers.
- Filler-related study. J Braz Plast Surg. 2018.
- Filler ultrasonography. Aesthet Surg J.
- Medicina review on fillers. Medicina. 2024;60:681.
- Ultrasound in dermal fillers.
- Recent filler study (2025).
- Suwanchinda A, et al. (2018).
- Ultrasound-guided filler management. Toxins. 2022;14:101.
6. 臉部血管解剖與安全 / Facial Vascular Anatomy & Safety
- Tansatit T, et al. (2019). Facial vascular anatomy.
- Tansatit T, et al. (2020). Facial vascular anatomy.
- Transverse facial artery: its role in blindness after cosmetic filler and botulinum toxin.
- Choi YJ, et al. (2018). Arterial anatomy.
- Park JT, et al. (2022). Superficial temporal artery and zygomatico-orbital artery. BioMed Res Int.
- Arterial anatomy study. J Tissue Neurol.
- Filler-related complication (10-1055-s-0040-1716185).
7. 上半臉:額肌 / Upper Face — Frontalis Muscle
- Frontalis muscle ultrasound anatomy. Toxins. 2025;17:594.
- Frontalis muscle study. Cureus. 2024;16:e63232.
- Meneses JV, et al. (2024). Increasing precision during neuromodulator injections for frontal rhytids. J Cosmet Dermatol.
- Frontalis study. Ultrasonics. 2019.
8. 上半臉:眶上區 / Upper Face — Supraorbital Region
- Supraorbital artery study. 2024;Article 4196.
- Erdogmus S, et al. (2007). Supraorbital anatomy.
- Supraorbital artery. Med Sci Monit. 2019;25:5201.
- Supraorbital region. Life. 2025;15:304.
9. 上半臉:眼周肌肉 / Upper Face — Orbicularis Oculi & Periorbital
- Ultrasonographic analyses of crow’s feet and novel guideline for botulinum toxin injection.
- Lateral eyebrow lifting and eye-opening point injection with botulinum neurotoxin: anatomical study.
- Upper face muscle ultrasound. Toxins. 2025;17:595.
10. 上半臉:皺眉肌、眉間 / Upper Face — Glabella
- Wu Y, et al. (2024). A prospective and randomized study comparing ultrasound-guided real time injection (glabella). J Cosmet Dermatol.
11. 上半臉:顳部(夫妻宮)/ Upper Face — Temple
- Breithaupt AD, et al. (2015).
- Sykes JM, et al. (2015).
- Suwanchinda A, et al. (2018). Temple injection.
- Kapoor KM, et al. (2020).
- Cotofana S, et al. (2020). 6 techniques for temple injection.
- Hernandez CA, et al. (2020).
- Temple filler safety. Front Plast Aesthet Surg. 2022.
- Temple anatomy. Front Surg. 2025;12:1603177.
- Yi KH, et al. (2025). Temporal fat pad filler injection for lifting purposes: shifting of the superficial temporal artery. J Cosmet Dermatol.
- Temple ultrasound. Life. 2025;15:266.
- Jiang J, et al. (2014). Middle temporal vein.
12. 唇部 / Lip
- Venous tributaries of the lip: implications for lip filler injection.
- Lip anatomy/ultrasonography. Life. 2025;15:315.
13. 埋線拉提 / Thread Lifting
- Thread lifting review. Plast Reconstr Surg Glob Open. 2019;7:e2045.
- Kim J, et al. (2023). Ultrasound-guided thread lifting for the prevention of parotid gland and facial nerve injury. Skin Res Technol.
14. 韌帶 / Retaining Ligaments
- Lores ligament study.
- Retaining ligaments / WJO. World J Orthop. 2018;9:227.
15. 肉毒桿菌素 / Botulinum Toxin (General)
- Toxins review. Toxins. 2022;14:101 (v2).
共計 75 篇文獻/教科書,依主題分為 15 類。 整理日期:2026-03-20
感謝Claude Code, ChatGPT, Gemini,這幾個月發現生產力增加許多,這個對地方爸爸幫助很多,也感覺能做一些野心更大的研究!